Fundamento teórico introdutório e terminologia
A NMR é uma técnica utilizada para analisar a estrutura de muitas moléculas químicas, sobretudo compostos orgânicos. Um composto típico pode ser constituído por átomos de carbono, hidrogénio e oxigénio.
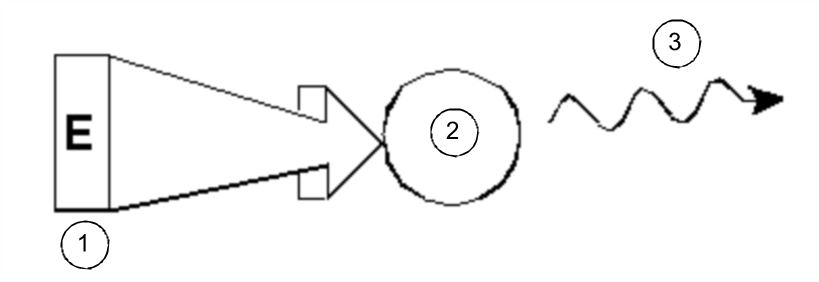
Na sua forma mais simples, uma experiência de NMR é constituída por três passos:
- 1.
- Colocar a amostra num campo magnético estático.
- 2.
- Excitar os núcleos na amostra com um impulso de radiofrequência.
- 3.
- Medir a frequência dos sinais emitidos pela amostra.
Excitação e resposta
A partir das frequências emitidas, os analistas podem deduzir informações acerca da ligação e disposição dos átomos na amostra. Os núcleos ativos de NMR na amostra apresentam ressonância de acordo com diversas frequências denominadas "frequências de ressonância“. São as frequências emitidas pelos núcleos quando estes são excitados pelo impulso de radiofrequência utilizado. O valor da frequência de ressonância depende de dois fatores:
1) Tipo de núcleo:
Cada isótopo apresenta uma combinação específica de protões e neutrões no núcleo. A estrutura do núcleo determina, em grande parte, o valor da frequência de ressonância. Assim, cada isótopo apresenta uma “frequência de ressonância básica”. Os núcleos de 13C apresentam uma frequência de ressonância básica diferente da obtida para o 1H, etc. Repare na variação ampla nas frequências de ressonância básicas entre os diferentes isótopos na tabela seguinte:
Tabela de dados para vários isótopos (frequências referentes a um íman de 11,7 T)
2) Ambiente atómico local:
O ambiente atómico local em que um isótopo está situado produz um efeito que se sobrepõe à frequência de ressonância básica. O valor preciso da frequência de ressonância de um núcleo de 1H num composto específico depende dos átomos a que este está ligado e que rodeiam o núcleo. O núcleo está rodeado por eletrões, os quais podem ser entendidos como cargas elétricas móveis com campos magnéticos associados. Estes eletrões funcionam como uma fonte de blindagem magnética para o núcleo. O grau de blindagem depende do ambiente atómico local preciso. A dimensão das variações típicas do campo local (que resultam numa variação da frequência) dependem do isótopo e da intensidade do campo magnético em que a amostra é colocada. A tabela seguinte apresenta a variação típica da frequência para dois dos núcleos mais amplamente utilizados em NMR, 1H e 13C. Podemos facilmente constatar que o ambiente atómico local tem um efeito relativamente pequeno na frequência de ressonância básica.
Variações da frequência (referentes a um íman de 11,7 T)
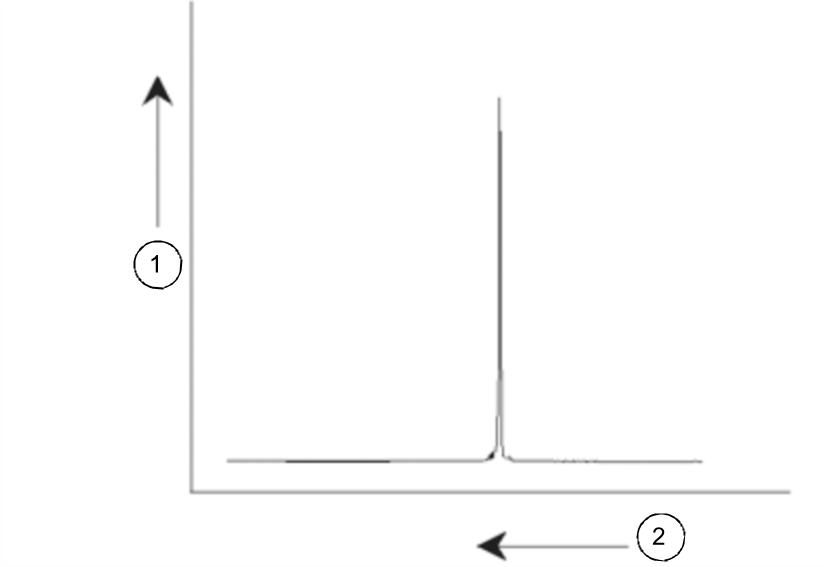
Os sinais de NMR são tipicamente traçados graficamente como espectros e analisados relativamente a duas características, frequência e intensidade. Na NMR convencional, a frequência é traçada no eixo horizontal, aumentando para a esquerda.
Espectro de NMR
Conforme foi mencionado acima, a frequência fornece informações qualitativas relativamente ao ambiente atómico local. A intensidadeintegrada de um sinal é uma medida daintensidade do sinal e é determinada pela integral da área sob o pico do sinal. A integral é diretamente proporcional ao número de núcleos que contribuem para um sinal numa frequência específica (se todos os núcleos forem igualmente excitados) e, desta forma, fornece informações quantitativas acerca da estrutura química.
Para excitar um determinado núcleo numa experiência de NMR, a frequência do impulso de excitação deve corresponder estreitamente à frequência de ressonância do núcleo. Esta frequência é designada por frequência portadora. Assim, se as experiências forem realizadas com um íman de 11,7 T, o núcleo de 1H requer uma frequência portadora de aproximadamente 500 MHz, enquanto que o núcleo de 13C requer uma frequência portadora próxima de 126 MHz. A frequência portadora é especificada pelo parâmetro SFO1. O núcleo excitado por esta frequência portadora designa-se o núcleo de observação.
Tenha em atenção que existem experiências em que é excitado mais do que um núcleo, por exemplo, durante a transferência de polarização ou desacoplamento. Nestes casos, existe mais do que uma frequência portadora mas continua a existir apenas uma frequência de observação.
Nem todos os isótopos reagem a impulsos de radiofrequência, ou seja, nem todos são ativos em NMR. Estão presentes três isótopos do elemento hidrogénio na natureza: 1H (hidrogénio), 2H (deutério) e 3H (trítio, radioativo!). A abundância natural destes isótopos é de 99,98%, 0,015% e 0,005%, respetivamente. Todos os três são ativos em NMR, embora apresentem uma frequência de ressonância muito diferente, conforme é indicado na tabela 3.1. Para analisar uma amostra de hidrogénio, o isótopo 1H é excitado, visto que é, de longe, o mais abundante. Entre os isótopos de carbono encontrados na natureza, apenas um é ativo em NMR. O isótopo mais comum, 12C (abundância natural de 98,89%), é inativo. Por este motivo, a análise de NMR de compostos orgânicos relativamente ao carbono dependem dos sinais emitidos pelo isótopo 13C, o qual tem uma abundância natural de apenas 1,11%. Por razões óbvias, a análise de NMR para o carbono é mais difícil do que, por exemplo, para 1H (existem outros fatores que afetam a sensibilidade, os quais são abordados nas secções seguintes deste capítulo).
Tendo em conta a breve introdução à NMR descrita acima, é um bom exercício ponderar a forma como a técnica pode ser utilizada para analisar a composição do clorofórmio (CHCl3).
Outras informações